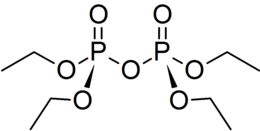
Тетраэтилпирофосфат
| Тетраэтилпирофосфат | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
Тетраэтилдифосфат |
| Сокращения | ТЭПФ |
| Традиционные названия | Тетраэтилпирофосфат |
| Хим. формула | C8H20O7P2 |
| Рац. формула | [C2H5O]4P2O3 |
| Физические свойства | |
| Состояние | бесцветная гигроскопичная жидкость |
| Молярная масса | 290,19 г/моль |
| Плотность | 1,189 г/см³ |
| Термические свойства | |
| Т. плав. | 0 °C |
| Т. кип. | 124 °C |
| Давление пара | 0,0002 ± 0,0001 мм рт.ст. |
| Оптические свойства | |
| Показатель преломления | 1,4071 |
| Классификация | |
| Рег. номер CAS | 107-49-3 |
| PubChem | 7873 |
| Рег. номер EINECS | 203-495-3 |
| SMILES | |
| InChI | |
| RTECS | UX6825000 |
| ChEBI | 82149 |
| Номер ООН | 3018 |
| ChemSpider | 7585 |
| Безопасность | |
| ЛД50 | 0,5 мг/кг (крысы, перорально) |
| Токсичность |
Чрезвычайно токсичен, сильнейший яд нервно-паралитического воздействия. 
|
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Тетраэтилпирофосфат, тетраэтилдифосфат, также тетраэтиловый эфир пирофосфорной кислоты (сокр. ТЭПФ) — фосфорорганическое соединение, сложный эфир, чрезвычайно токсичное вещество, обладает необычайно сильным контактным инсектицидным воздействием, относится к группе тетраалкилдифосфатам. Токсичность ТЭПФ, как и многих других ФОС обусловлена необратимым ингибированием фермента ацетилхолинэстеразы, а также некоторых сериновых протеаз (химотрипсин и другие), в крайне низких концентрациях (10-5—10-8 М и менее), вызывая патофизиологические эффекты со стороны ЦНС (судороги, кинетозы, спазмы, параличи, нарушения сознания, кому), сердечно-сосудистой (брадикардия, резкое падение артериального давления, коллапс), пищеварительной систем (слюнотечение, рвоту, диспептические явления итд.), дыхательной (бронхоспазм), и как следствие летальный исход. Вследствие этих негативных свойств имеет запрет на производство и применение в России.
Содержание
Физико-химические свойства
Представляет собой бесцветную или слегка желтоватую (технический препарат) легкоподвижную жидкость, с приятным запахом, хорошо растворимую в воде, также растворяется в органических растворителях: в бензоле, толуоле, тетрахлорметане, ацетоне, этаноле, плохо растворяется в лигроине и петролейном эфире. Ввиду высокой гигроскопичности ТЭПФ неустойчивое соединение и быстро гидролизуется (~7 ч при 25 °С) до низкотоксичных продуктов (диэтилфосфорная кислота). При нагревании свыше 170 °С ТЭПФ разлагается, а при температуре свыше 208 °С происходит бурное выделение этилена.
Получение
ТЭПФ был одним из первых синтезированных ФОС. Впервые синтез осуществлён Мошниным в 1850 году, в лаборатории Ш. Вюрца (Париж). В 1854 году Ф. Клермонт синтезировал эфир из серебряной соли пирофосфорной кислоты и йодистого этила по схеме:
В СССР впервые синтез ТЭПФ произведен в химическом институте Казанского филиала АН СССР А.Е. Арбузовым в 1931 году.
Применение
Ввиду чрезвычайно высокой токсичности ТЭПФ применение ограничено, в настоящее время его используют в качестве инсектицидных смесей с другими ФОС. Как боевое отравляющее вещество ТЭПФ не может быть использовано, вследствие низкой устойчивости и быстрому гидролизу (оно практически неэффективно во влажном климате).
Эффективность как пестицида
ТЭПФ является одним из первых фосфорорганических инсектицидов и акарицидов с чрезвычайно сильным контактным воздействием (даже в ничтожных концентрациях — 0,02% и менее вызывал полную гибель тли и клещей), более сильным, чем никотин. Несмотря на это, ТЭПФ не оказывает системного воздействия, то есть не распространяется по организму насекомого. ТЭПФ можно использовать в качестве эффективного фумиганта (препарат находится в форме аэрозоля). Растения, опрыскиваемые ТЭПФ через сутки становятся безопасными, так как он полностью гидролизуется.
Технический препарат, содержащий до 40% ТЭПФ называют бладан. Впервые использован как инсектицид в 1943 году в Германии.
Синонимы и торговые названия
- Бладан (продукт компании «Фарбенфабрике Байер», ФРГ),
- Вапотон (California spray-chemical Co, США),
- Киллакс,
- Мортопал,
- Нифос Т (Монсанто, США),
- Тетрон (American Potash and Chemical Company, CША).
Токсикология и безопасность
ТЭПФ типичный представитель фосфорорганических соединений с ярко выраженным антихолинэстеразным воздействием.
Молекулярный механизм действия ТЭПФ
Действие молекул ТЭПФ на активный центр холинэстеразы, как и всех сериновых протеаз основан на связывании серина и образования с ним ковалентно прочного тераэтилсеринпирофосфата, который очень слабо гидролизуется, тем самым изменяет конформацию фермента, приводя его в неактивную форму. Инактивация сериновых протеаз ТЭПФ наблюдается даже в крайне низких концентрациях.
Токсичность
ТЭПФ чрезвычайно токсичное вещество. ЛД50 даны в таблице.
| Организм | ЛД50 в мг/кг |
|---|---|
| Крысы | 0,5-1,7 (перорально) |
| Мыши | 5-7 (внутрибрюшинно) |
| Кролики | 6-7 (накожно) |
| Кошки | 1,2-3 (накожно) |
| Человек | 0,7-1 (перорально) <0,4 (аэрозоль) |
Смертельная доза для человека при пероральном поступлении ТЭПФ составляет порядка 80-100 мг. Наибольший токсический эффект развивается при вдыхании паров или аэрозоля ТЭПФ. ЛД100 при респираторном пути проникновения снижается до 15-30 мг.
Основные пути проникновения ТЭПФ в организм человека — респираторный (дыхательный), пероральный или контактный (накожный). Признаки отравления могут возникнуть в течение нескольких минут. Признаками отравления служат резкое увеличение потовыделения, миоз (сужение зрачков), слюнотечение, головокружение, снижение мышечной активности (миастения), гипотония, брадикардия, поражение зрения, судороги, диспептические явления, тошнота, рвота, понос, бронхоспазм в случае вдыхании аэрозоля или паров. При высоких дозах (40-70 мг) происходит почти мгновенное поражение ЦНС, потеря сознания, конвульсии или параличи, как следствие кома, возможен летальный исход в течение нескольких часов.
Эффективными антидотами при отравлении ТЭПФ служат атропин и 2-ПАМ (пралидоксим).
Безопасность
ТЭПФ относится к веществам с очень высокой опасностью (I класс опасности). В России данное вещество запрещено в производстве и применении. В США ПДК составляет 0,05 мг/м3.
